腸道菌群對宿主生理有著廣泛影響,目前研究多關注於菌群代謝物進入血液循環後的生理效應,而其在腸道,這一菌群-宿主互作界麵的效應則少有研究。機體進食後腸道上皮中的內分泌細胞產生的多種腸促胰島素(incretin),調控機體代謝平衡。其中胰高血糖素樣肽(GLP-1),可以促進胰腺中胰島素的分泌、延緩腸道蠕動性並抑製食欲。GLP-1受體激動劑已成功應用於2型糖尿病和肥胖症的臨床治療。
2024年07月19日,万博英超狼队网官方网 於肖飛團隊在Nature Metabolism發表了題目為Hydrogen sulfide produced by the gut microbiota impairs host metabolism via reducing GLP-1 levels in male mice的文章,報道了以脫硫弧菌(Desulfovibrio)為代表的腸道菌可通過產生硫化氫抑製GLP-1的產生,並促進肥胖等代謝疾病的發生,從而揭示了腸道菌通過腸道“中繼”影響機體代謝的新通路。由腸道菌群領域著名專家、美國RUTGERS大學趙立平教授撰寫的評述文章“'H2S as a metabolic saboteur”也同期上線。

團隊在早期進行免疫-代謝交叉研究時,發現免疫缺陷的TCRb-/-小鼠體內的GLP-1水平顯著升高,且該效應有腸道菌群引起。通過高通量16S和宏基因組測序,團隊發現脫硫弧菌Desulfovibrio desulfuricans與體內GLP-1水平呈顯著負相關,並在高脂飲食誘導肥胖小鼠及公開的人群幹預實驗中得到驗證(Zhao et al., Science, 2018)。
隨後團隊以Desulfovibrio desulfuricans DSM642作為代表性菌株進行後續研究, 發現Desulfovibrio定植可顯著降低小鼠體內的GLP-1水平,且伴隨糖耐量受損。通過建立新的GLP-1細胞模型(GLARE),團隊發現Desulfovibrio產生的H2S可通過抑製線粒體功能並激活未折疊蛋白反應(UPR)的IRE1a通路,降低GLP-1的分泌和基因轉錄。為驗證H2S對GLP-1的調控作用,團隊利用合成生物學方法改造大腸杆菌,使之能夠產生H2S,發現其在體外與體內均可以抑製GLP-1的產生。最後,團隊利用非處方(OTC)藥,次水楊酸鉍(Bismuth Subsalicylate),螯合小鼠腸道中的硫化氫,發現其可顯著降低腸道中H2S濃度、提高GLP-1水平、減緩肥胖的發生,並伴隨糖耐量的明顯改善。
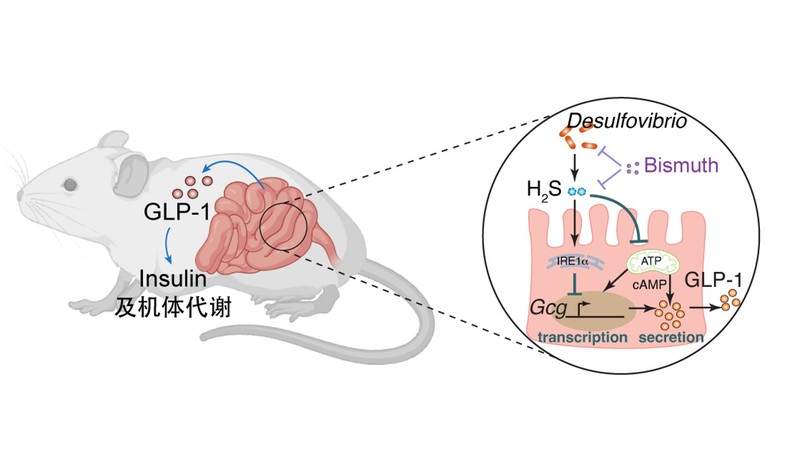
圖:Desulfovibrio產生H2S抑製腸道內GLP-1進而影響機體代謝分子機製示意圖
綜上,該項工作通過腸道菌群和宿主分子-細胞-機體水平的係統研究,揭示了腸道菌產生的硫化氫通過抑製腸道內GLP-1的產生而損害機體代謝,為腸道菌群通過腸道“中繼”信號加重代謝疾病提供了新證據。與此同時,使用非處方藥次水楊酸鉍可以通過螯合腸道內硫化氫進而增強機體血糖調節從而延緩肥胖等代謝類疾病的進程,為肥胖等代謝類疾病的治療提供了新的思路。
万博英超狼队网官方网 、複旦微生物組中心於肖飛研究員為最後通訊作者,耶魯大學醫學院Marc Schneeberger教授、上海交通大學醫學院附屬仁濟醫院陳磊研究員為共同通訊作者。万博英超狼队网官方网 博士生齊晴晴、張慧潔、金哲宇為論文的共同第一作者。
文章鏈接:https://www.nature.com/articles/s42255-024-01068-x

